FÍSICAMENTE: Desde el punto de vista físico, el agua circula constantemente en un ciclo de evaporación o transpiración (evapotranspiración), precipitación, y desplazamiento hacia el mar. Los vientos transportan tanto vapor de agua como el que se vierte en los mares mediante su curso sobre la tierra, en una cantidad aproximada de 45.000 km³ al año. En tierra firme, la evaporación y transpiración contribuyen con 74.000 km³ anuales al causar precipitaciones de 119.000 km³ cada año.
QUÍMICAMENTE: casi la totalidad de los procesos químicos que ocurren en la naturaleza, 831 como los que se realizan en el laboratorio, tiene lugar entre sustancias disueltas esto entre soluciones acuosas. Su fórmula química es H2O, protóxido de hidrogeno formado al combinarse dos volúmenes de hidrogeno por uno de oxígeno, se presenta en la naturaleza en estado sólido como el hielo, nieve, escarcha y neviza, Liquido en lluvias, mares etc., .gaseoso en vapor de agua. el agua se trata de un compuesto extremadamente complejo (hay que tener en cuenta los isótopos del hidrógeno y del oxígeno) y del que, en la actualidad, no se puede tener una idea clara sobre su naturaleza y sus agrupaciones moleculares. Además es un compuesto polar, lo que hace que todas sus constantes físicas sean anormales.
BIOLOGICAMENTE: Es esencial para la supervivencia de todas las formas conocidas de vida. El término agua, generalmente, se refiere a la sustancia en su estado líquido, pero la misma puede hallarse en su forma sólida llamada hielo, y en forma gaseosa denominada vapor. El agua cubre el 71% de la superficie de la corteza terrestre.2 Se localiza principalmente en los océanos donde se concentra el 96,5% del agua total, los glaciares y casquetes polares poseen el 1,74%, los depósitos subterráneos (acuíferos), los permafrost y los glaciares continentales suponen el 1,72% y el restante 0,04% se reparte en orden decreciente entre lagos.
2. ESTRUCTURA DEL AGUA , PUENTES DE HIDROGENO , POLARIDAD DE AGUA.
La configuración más común de las moléculas de agua líquida es tetraédrica con dos átomos de hidrógeno unidos covalentemente al oxígeno y otros dos hidrógenos unidos por enlaces de hidrógeno. Ya que los enlaces de hidrógeno varían en longitud muchas de estas moléculas de agua no son simétricas y forma tetraedros irregulares transitorios entre sus cuatro átomos de hidrógeno asociados.2 Cuando la molécula de
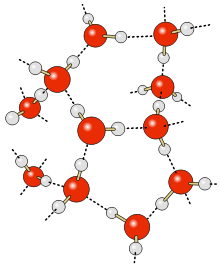
Los puentes de Hidrógeno, se forman por átomos de Hidrógeno localizados entre átomos electronegativos. La estructura del agua favorece las interacciones para formar puentes de Hidrógeno, el arreglo siempre es perpendicular entre las moléculas participantes, además, es favorecido por que cada protón unido a un Oxígeno muy electronegativo encuentra un electrón no compartido con el que interactúa uno a uno. De lo anterior se concluye que cada átomo d Oxígeno en el agua interacciona con 4 protones, dos de ellos unidos covalentemente y dos a través de puentes de Hidrógeno.
La polaridad química o solo polaridad es una propiedad de las moléculas que representa la separación de las cargas eléctricas en la misma. Esta propiedad está íntimamente relacionada con otras propiedades como la solubilidad, punto de fusión, punto de ebullición, fuerzas intermoleculares, etc.
Al formarse una molécula de modo covalente el par de electrones tiende a desplazarse hacia el átomo que tiene mayor electronegatividad. Esto origina una densidad de carga desigual entre los núcleos que forman el enlace (se forma un dipolo eléctrico). El enlace es más polar cuanto mayor sea la diferencia entre las electronegatividades de los átomos que se enlazan; así pues, dos átomos iguales atraerán al par de electrones covalente con la misma fuerza (establecida por la Ley de Coulomb) y los electrones permanecerán en el centro haciendo que el enlace sea apolar.
3. CLASES DE AGUA
Agua dulce
Agua dura
Agua blanda
Aguas negras
Aguas grises
Aguas residuales
Aguas residuales municipales
Agua bruta
Aguas muertas
Agua alcalina
Agua capilar
Agua de adhesión
Agua de desborde
Agua de formación
Agua de gravedad
Agua de suelo
Agua disfórica
Agua estancada
Agua fósil
Agua freática
Agua funicular
Agua primitiva
Agua magmática
Agua metamórfica
Agua vadosa
Agua subterranea
El agua según sus propiedades para el consumo se divide en potable y no potable.
Según la cantidad de minerales se la considera dura o blanda.
Según la procedencia puede ser superficial o subterranea
Las aguas embotelladas suelen proceder de manantiales ricos en minerales de ahí que se la conozco, en general, como agua mineral.
Acidez y Basicidad del agua
La cesión de protones por un ácido y la aceptación de protones por una base son procesos reversibles. Dado que este tipo de procesos desembocan al cabo de un cierto tiempo en una situación de equilibrio, su estudio puede efectuarse aplicando los conceptos fundamentales del equilibrio químico.
El equilibrio ácido-base más sencillo y fundamental a la vez es el que corresponde a la disociación del agua:
H2O + H2O «-- H3O+ OH-Base 1 ácido 2 ácido 1 base 2 Esta reacción pone de manifiesto que el agua puede actuar como una base (base 1) ganando protones para convertirse en H3O+ (ácido 1) y puede actuar como un ácido (ácido 2) perdiendo protones para convertirse en OH- (base 2). Se dice por ello que es una sustancia anfolita.Como pone de manifiesto la escasa conductividad del agua pura, el equilibrio iónico del agua está considerablemente desplazado hacia la izquierda, lo que significa que, de acuerdo con la ley de acción de masas, su constante de equilibrio K es muy pequeña:En el agua pura la presencia de iones H3O+ y OH- procede únicamente de su disociación iónica, por lo que sus concentraciones respectivas son iguales.
Proceso de purificación del agua:
 El agua purificada se obtiene mediante varios procesos de purificacion, contrario a lo que se puede pensar, ya que antes el agua solo se "filtraba" y estaba lista para tomar, hoy en dia no solo se debe filtrar, pues la filtracion es solo eliminar particulas suspendidas en el agua como tierra, estos contaminantes son los mas inofensivos, por lo que actualmente se deben eliminar mucho mas contaminantes del agua.
El agua purificada se obtiene mediante varios procesos de purificacion, contrario a lo que se puede pensar, ya que antes el agua solo se "filtraba" y estaba lista para tomar, hoy en dia no solo se debe filtrar, pues la filtracion es solo eliminar particulas suspendidas en el agua como tierra, estos contaminantes son los mas inofensivos, por lo que actualmente se deben eliminar mucho mas contaminantes del agua.Algunos procesos de purificación:
Cloracion-Desinfeccion-del-agua
Filtracion-lecho-profundo
Filtracion-por-carbon-activado
FIltracion-por-cartucho-5 micras
Suavizacion-del-agua
Osmosis-inversa-ultrapurificacion
Pulido-agua-1-micra
Luz-ultravioleta-esterilizacion
ozonacion-del-agua
Lavado de garrafon
Llenado-de-garrafon
Desinfección Solar de Aguas (Sodis)
Una tecnología ya bien establecida y aceptada para proveer agua bacteriológicamente segura que se basa en la exposición al sol de la botella conteniendo el agua contaminada por aproximadamente seis horas.
Los rayos solares actúan por combinación de la radiación UV-A y la radiación infrarroja destruyendo bacterias y virus (incluyendo al vibrio cholerae).
Esta técnica es universal, altamente probada.
La única restricción es que el agua se debe tomar durante ese día, de lo contrario los microorganismos se vuelven a reproducir.
Remoción de Arsénico por Oxidación Solar modificada
El agua se coloca con algunos gramos de alambre (por ejemplo, de enfardar) o lana de acero (virulana), que se irradia por algunas horas. Este tratamiento elimina el arsénico por oxidación y coprecipitación con óxido de hierro formados en el proceso. Por la noche, la botella se deja en posición vertical para promover la precipitación y por la mañana se filtra por un paño de tela, similar al que se usa para el café.
La tecnología Soras fue probada con bastante éxito en la India y Bangladesh, entre otros países. Sirve para eliminar el arsénico 3, pero no para el arsénico 5 (de alta prevalencia en Argentina).
Para que Soras sea efectivo en países con arsénico 5, como Argentina se necesita que el agua tenga más hierro. Por eso, lo debemos agregar externamente, con alambre o virulana. Estos compuestos forman unos ‘barros’ sobre los cuales se absorbe o coprecipita el arsénico”.
Fotocatálisis heterogénea solar con TiO2 (FH)
Es una tecnología avanzada de oxidación que emplea una sustancia barata, reutilizable y no tóxica, el dióxido de titanio que elimina compuestos orgánicos tóxicos, metales como cromo o arsénico, y hasta puede destruir bacterias y virus. En este caso, las botellas se colocan al sol con el agua y el fotocatalizador (TiO2) fijado a sus paredes por un procedimiento muy simple, que podría ser efectuado por los mismos pobladores, adecuadamente instruidos para ello.
En esta técnica podría eliminar todo el arsénico, la contaminación microbiana, orgánica y probablemente el uranio (aunque los estudios no han finalizado).
El dióxido de titanio está presente en los jugos sintéticos, tipo Tang (se usa como espesante), también en cosméticos y pantallas solares.
El procedimiento consiste en hacer una pequeña capa de este dióxido, un especie de film, que se coloca en el interior de la botella. El mismo le da opacidad y se estima que expuesto a la energía solar podría eliminar todos los tóxicos.
Ejemplo: Un trabajo realizado en Tucumán (Argentina) con agua contaminada con un herbicida muy difundido (2,4-D). Se aplicó esta técnica y toda la materia orgánica se transformó en dióxido de carbono (CO2). O sea, se produjo una descontaminación. Lo mismo hace con un microorganismo; que lo inactiva y lo mineraliza. Uno de los inconvenientes es que el proceso de exposición requiere una exposición bastante prolongada a la radiación solar. Aún no se cuenta con valores recomendados.
EL HIDRATO EN EL AGUA:
En química orgánica, un hidrato es un compuesto formado por el agregado de agua o sus elementos a una molécula receptora. Por ejemplo, el etanol, C2—H5—OH, puede ser considerado un hidrato de etileno, CH2=CH2, formado por el agregado de H a un C y OH al otro C. Una molécula de agua puede ser eliminada, por ejemplo mediante la acción de ácido sulfúrico. Otro ejemplo es elhidrato de cloral, CCl3—CH(OH)2, que puede ser obtenido mediante la reacción de agua con cloral, CCl3—CH=O.
En química inorgánica, los hidratos contienen moléculas de agua que o bien están ligadas a un núcleo metálico o están cristalizadas con el complejo metálico. Tales hidratos se dice que poseen "agua de cristalización" o "agua de hidratación". Ésta es liberada cuando el hidrato es sometido a alta temperatura, la red se rompe y deja escapar una o más moléculas de agua. Si el agua es agua pesada, donde el hidrógeno consiste del isótopo deuterio, entonces se suele utilizar el términodeuterar en lugar de hidratar.
Actualmente la industria utiliza el 22% del agua consumida en el mundo. En los países ricos ese porcentaje asciende a un 59%, mientras que en los países pobres sólo llega a un 8%. En el año 2.025 esa proporción alcanzará un 24%. Se calcula que para ese entonces se gastarán 1.170 km³ de agua anuales para usos industriales.
Cuando faltan las infraestructuras y los servicios, las áreas urbanas que careen de instalaciones para el suministro y el saneamiento de aguas constituyen uno de los entornos más peligrosos para la vida humana. Muy pocas viviendas en esta Tierra tienen desagües que vayan a parar al alcantarillado. La población pobre que vive esa situación en las ciudades es la primera víctima de las afecciones causadas por la falta de saneamientos, las inundaciones e, incluso, por las enfermedades causadas por el agua como la malaria, que se ha convertido en una de las principales causas de enfermedad y muerte en muchas áreas urbanas. Por otro lado, a medida que la demanda de agua aumenta, proliferan también los rumores sobre las guerras que pueden avecinarse debido a la falta de los recursos hídricos.
De todas las crisis sociales y naturales que debemos afrontar los seres humanos, la de los recursos hídricos es la que más afecta a nuestra propia supervivencia y a la del planeta. Ninguna región del mundo podrá evitar las repercusiones de esta crisis que afecta a todos los aspectos de vida, desde la salud de los niños hasta la alimentación de los seres humanos. Los abastecimientos de agua disminuyen, mientras que la demanda crece a un ritmo pasmoso e insostenible. Se prevé que en los próximos veinte años el promedio mundial de abastecimiento de agua por habitante disminuirá en un tercio.
La falta de consciencia sobre la magnitud del problema, la inercia de los dirigentes y las actitudes y conductas inapropiadas explican el deterioro progresivo de la situación y la razón de por qué no se adoptan las medidas que se necesitan.
A mediados del presente siglo miles de millones de personas sufrirán de escasez de agua en todo el mundo. Se calcula que un 20% del incremento de la escasez mundial de agua obedecerá al cambio climático. En las zonas húmedas es probable que las precipitaciones lluviosas aumenten, mientras que en muchas zonas propensas a la sequía, e incluso en algunas regiones tropicales y subtropicales, disminuirán y serán más irregulares. La calidad del agua empeorará con la elevación de su temperatura y el aumento de los índices de contaminación. Ya en los últimos años se ha evidenciado una importante disminución en su calidad. Y los más afectados siguen siendo los pobres, ya que el 50% de la población de los países subdesarrollados está expuesta al peligro que representan las fuentes de agua contaminadas.
Otros problemas muy importantes que se plantean son los de la calidad y la buena administración del agua. En el mundo hay más de 2,2 millones de personas que mueren cada año debido a enfermedades causadas por el agua potable contaminada y un saneamiento deficiente. Una gran proporción de esas muertes se debe a las enfermedades ocasionadas por el agua. Aproximadamente, un millón de personas muere de malaria cada año y más de 200 millones se ven aquejadas de esquistosomiasis, una dolencia conocida también con el nombre de bilharziosis. Todas estas terribles desgracias, así como los sufrimientos y pérdidas que entrañan, se pueden evitar
No hay comentarios:
Publicar un comentario